PLAN DE MEJORAMIENTO DE QUÍMICA - GRADO 11
Instrucciones y Orientaciones
-Resolver los cuatro talleres propuestos de química.
- Utilice los talleres que están publicados en la plataforma institucional o en el blog: cienciasada.blogspot.com para resolver las actividades propuestas.
- La presentación es en físico, debe realizarlo a mano en hojas de block, cada una de las hojas debe estar marcada con su nombre y grado, debe llevar una portada al inicio.
- El taller puede ser enviado al correo ayascual@gmail.com o enviarlo por whatsapp
- Deberá sustentarlo en el mes de enero 2021, se acordará la fecha.
Taller 2 -Primer Periodo. Gases
ACTIVIDAD
1. Resuelva los siguientes ejercicios sobre las leyes de los gases e
indique a que ley hace referencia, los datos del problema y la respectiva
fórmula:
NOTA: recuerde que la temperatura se debe trabajar en Kelvin. (K= 273 + °C)
a. La presión de cierta cantidad de ácido sulfhídrico (H2S) a 20°C es de 625 torr. Cuál es su presión a 80°C. Si el volumen permanece constante.Rta:752 torr
b. Un globo se infla hasta un volumen de 2,5 L en una habitación caliente a 30°C, entonces se saca el globo a una temperatura externa de -25°C. Suponiendo que la presión se mantiene constante. Cuál será el volumen del globo cuando este afuera. Rta: 2,04 L
c. Un globo se infla con hexafluoruro de azufre (SF6), el cual es un gas incoloro e inodoro muy poco reactivo. Este gas se encuentra ocupando un volumen de 5 L. Si 3 moles de este gas tienen una presión de 2,6 atm. Que temperatura tendrá el gas. Rta:52K
d. Un recipiente contiene 0,6 m3 de un gas a 5 atm. Calculemos el volumen que ocupará el gas si aumenta la presión a 6 atm, sin variar la temperatura.Rta:0,5 m3
e. Si 35 L de dióxido de carbono (CO2) se encuentran en condiciones de temperatura y presión ambiente de 20 °C y 560 mmHg respectivamente. Cuál será su volumen a 0°C y 760 mmHg de presión. Rta: 24 L
2. Indique que sucede en cada situación (aumenta, disminuye):
a. al calentar un gas que sucede con el movimiento de las moléculas del
gas:__________
b. al aumentar la presión de un gas que sucede con los choques contra el
recipiente:____________
c. al disminuir la temperatura que sucede con el movimiento de las
moléculas del gas:____________
d. al disminuir la temperatura que sucede con los choques contra las
paredes:__________
e. al disminuir la temperatura que sucede con la presión:__________
f. Que sucede con el volumen del gas al disminuir la presión:__________
g. Que sucede con el volumen del gas al disminuir la temperatura:___
Taller 1 -Segundo Periodo. Unidades de Concentración de las Soluciones
ACTIVIDAD
1. Cuál es la molaridad de una solución. Si 500ml contienen 4 g de NaOH.
Rta: 0,2mol/L
2. Se tiene una solución 0,750 molar de ácido fosfórico (H3PO4).Cuántas
moles del ácido contiene y en que volumen de sln.
3. Se tiene una solución de KCl 17% m/m. Cuál es la masa de
soluto, masa del solvente y masa de la solución.
4. una solución de bromuro de sodio (NaBr) contiene 116 g de la sal por
cada 100 g de agua. Cuál es el % m/m. Rta: 53,7%
5. Se prepara una solución disolviendo 5 g de yoduro de potasio (KI) en agua suficiente para obtener 250 ml de solución. Calcular su concentración expresada en porcentaje masa/volumen (%m/v). Rta: 2%
6. Si se disuelven 10 g de potasa caustica (KOH) en 450 mL (450 g) de
agua. Cuál es la concentración molal de la solución. Rta: 0,4 molal
ACTIVIDAD
1. La solubilidad del KMnO4 a 60°C es S= 22,2 g/100
g H2O. Teniendo en cuenta la información responde las
preguntas:
a. Cuál es la temperatura:
b. Cuántos g o ml de agua se tienen:
c. Cuántos g de KMnO4 se disuelven:
d. sto:
e. ste:
2. Se tienen 50 g de AgNO3 en 100 ml de agua a 20°C. (La
solubilidad del AgNO3 a 20°C es S= 225 g/100 g H2O)
a. la solución es saturada o insaturada:
b. La solución es diluida o concentrada:
3. Se tienen 20 g de KMnO4 en 100 ml de agua a 60°C. (La
solubilidad del KMnO4 a 60°C es S= 22,2 g/100 g H2O)
a. la solución es saturada o insaturada:
b. La solución es diluida o concentrada:
4. Se tienen 67 g de KBr en 100 ml de agua a 20°C. (La solubilidad del
KBr a 20°C es S = 67 g/100 g H2O)
a. la solución es saturada o insaturada
5. Ordene, de menor a mayor, las siguientes soluciones según la
concentración:
a. 0.1 g de KMnO4 en 100 g de H2O a
20°C
b. 22 g de KMnO4 en 100 g de H2O a 20°C
c. 1 g de KMnO4 en 100 g de H2O a 20°C
6. Explica cada una de las siguientes situaciones utilizando uno de los
factores que afectan la solubilidad.
a. Cuando el agua se calienta pierde el oxígeno favoreciendo la
contaminación del agua.
b. Al servir algunas gaseosas, se observan burbujas que salen del
líquido
c. El azúcar que se utiliza para endulzar el café esta pulverizada
d. Al preparar el café, el azúcar se disuelve más rápido, si está
caliente.
e. Al preparar el café utilizamos una cuchara para disolver el azúcar
f. Se prepara una mezcla de aceite y agua, y otra de alcohol y agua. Por qué el alcohol se disuelve en el agua y el aceite no?
Taller 3 -Segundo Periodo. Los Hidrocarburos
ACTIVIDAD 1
1.
Escriba formula estructural desarrollada, condensada y molecular para:
a. la serie homologa (compuestos que tienen el mismo grupo funcional diferenciandose en un átomo de C) del metano hasta el pentano.
2.
Elabore la estructura de los siguientes compuestos:
a.
2,6-dimetil-5-propil-3,4-octadieno
b.
3-etil-2,5-dimetilhexano
c.
3-octino
d.
1,2-dimetilciclopentano
e.
m-butiletilbenceno
f. 2-etil-1-isopropil-3-metilbenceno
g. 2-metil-3-hexeno
h. etilbenceno
3.
Nombre las siguientes compuestos:
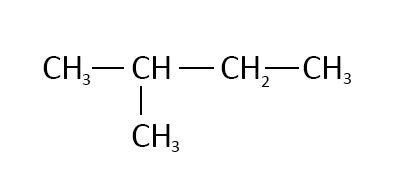 b
b d.
d.
No hay comentarios:
Publicar un comentario